发布时间:2023-09-11 作者:原博士带你做检测 浏览:1
中华检验医学培训工程专家委员会,中华医学会呼吸病学分会共同发布了“成人呼吸道感染病原诊断核酸检测技术临床应用专家共识(2023)”这个专家共识堪称目前最全面的核酸检测技术应用指南,不光详细介绍了每种核酸检测技术的优缺点,并且采用基于检测技术和基于应用场景两个维度将检测技术和应用场景进行融合,更具有指导价值。本文将侧重于检测技术方面对该专家共识进行解读。

一、核酸检测技术
1 实时荧光PCR 技术
实时荧光PCR 技术是一种可对核酸进行定量的试验方法,其原理主要是通过实时采集荧光信号对核酸扩增进行监测。在PCR 扩增的指数时期,模板的Ct值与其起始拷贝数存在线性关系,可实现对未知样本的定量检测。
1.1 临床应用场景
主要适用于门急诊、住院患者和大人群筛查,基于分子检验平台进行病原体(包括病毒、细菌、真菌、非典型病原体)的核酸检测,检测标本类型以鼻咽拭子、痰和支气管肺泡灌洗液(BALF)为主。
1.2 技术特点
作为传统的经典定量分析方法,荧光探针法的灵敏度和特异度明显优于底物发光法,但特异性引物探针的成本和对仪器的要求较高。其结果判读较为复杂,需要对扩增曲线和熔解曲线进行分析。
1.3 性能验证要求
定量检测需验证的性能指标包括:正确度、精密度(包括测量重复性和测量中间精密度)、不确定度、特异度(包括抗干扰能力)、灵敏度、检出限、定量限、线性区间(可报告区间)等。
定性检测需验证的性能指标包括:方法符合率、检出限、抗干扰能力、交叉反应等[8],具体性能指标以产品说明书要求为准。
1.4 专家推荐意见
实时荧光PCR 包括单靶标或多靶标呼吸道病原体核酸检测,可作为核酸即时检测法的参考方法,主要适用于门急诊、住院患者和大规模人群筛查
原博士:本文中提到“实时荧光PCR 技术是一种可对核酸进行定量的试验方法”是有误的,实时荧光PCR 技术只能进行间接定量,即定性检测。用实时荧光PCR 进行定量性能指标验证基本是不可能完成的。
对实时荧光PCR 技术进行定性检测的验证指标应包括:精密度、分析敏感性(检出限)、分析特异性(交叉反应、干扰试验)、临床符合率(诊断敏感性和诊断特异性)。
2 等温扩增技术
相较传统PCR 变温技术,等温扩增技术通常不需要改变反应温度,该技术方案多、技术原理差异较大,且各具优势,但基本原理仍是以特异性酶和引物进行扩增。等温扩增技术大多为指数扩增,目前多为定性检测[9]。2.1 应用场景
主要适用于发热门诊、急诊患者上呼吸道感染病毒(如新型冠状病毒、流感病毒等)及下呼吸道感染细菌(如肺炎链球菌、金黄色葡萄球菌、肺炎克雷伯菌等)的快速筛查。
2.2 技术特点
等温扩增反应通常耗时短,扩增效率高,不需要PCR 循环仪[10]且操作简单,但由于其技术的复杂性,尚难以全部直接用于临床。
技术局限性:(1) 在引物设计上,环介导等温扩增技术、交叉引物扩增技术、链置换扩增、重组酶聚合酶等温扩增技术等较为复杂,且引物数量通常>4 条;而滚环核酸扩增技术和解旋酶依赖性扩增技术则相对容易;(2)需要额外进行核酸提取。
2.3 性能验证要求
通常等温扩增为定性实验,需满足中国合格评定国家认可委员会GL039[11]定性实验的验证要求:符合率≥90%;阴性和弱阳性样本精密度检测结果完全一致;参照厂家说明进行靶基因检测,5 次重复检测应100%检出,20 次重复检测应检出至少18 次。
2.4 专家推荐意见
等温扩增耗时短、扩增效率高,通常以核酸即时检测的形式出现,适用于门急诊、发热门诊呼吸道感染患者病原体核酸快速筛查。
原博士:等温扩增优势很显著:仪器简单、操作简单、快;劣势也很显著:设计复杂、成本高、准确性上不如实时荧光PCR。
性能验证上说需满足“CNAS GL039 分子诊断检验程序性能验证指南”,指南里,定性项目的性能验证包括:方法符合率、检出限、抗干扰能力、交叉反应,为什么还少了后两项呢?
3 数字PCR 技术
数字PCR 是一种不依赖于核酸外标的核酸绝对定量技术[12]。其原理是通过微流控技术,将目标核酸和PCR 反应液分布在多个反应单元内进行PCR 扩增,以液滴形式进行检测的方式也被称为微滴数字PCR。该技术通过检测扩增后每个反应单元的荧光信号强度,判断含有目标核酸的反应单元个数,基于泊松分布计算起始样本中的目标核酸分子数,实现对核酸浓度的绝对定量。
3.1 应用场景
可直接定量检测样本中病原体个数,特别适用于低浓度样本、低丰度基因或突变基因的检测,也可作为质控方法评估其他分子检测产品的扩增效率。
3.2 技术特点
无需标准曲线和标准品,可有效降低临床样本复杂本底对扩增的干扰,具有良好的重现性和准确度。其主要影响因素是PCR 扩增和荧光信号分析,前者与PCR 扩增效率、扩增体系的配置有关;后者与检测器的灵敏度、核酸拷贝数、被分割成的物理单元数以及反应单元数有关,反应单元数越多,灵敏度越高。
技术局限性:(1)不同数字PCR 采用的微流控单元分割技术和耗材试剂具有封闭性,不同厂家试剂和平台的检测结果存在差异,尚无可评估其定量结果准确性的跨平台质控技术及非数字PCR 方法学质控;(2)依托荧光探针进行定量检测的方法受限于靶标通量;(3)由于该技术检测灵敏度为单分子水平,不适用于检测浓度相对较高的样本;(4) 数字PCR 报告审核规则,尤其是低丰度检测结果的报告原则,尚无定论。
3.3 性能验证要求
应使用泊松分布计算靶标分子拷贝数,不同荧光通道之间应不存在相互干扰。定量检测性能指标应包括:反应单元体积精密度、准确度、有效率;样本检测重复性、线性、动态范围、灵敏度。基于芯片的数字PCR 芯片内应无气泡,阳性和阴性的随机分布应得到视觉确认。微滴数字PCR 单次反应生成的最小液滴数应符合厂商建议或用户自定义值[13]。
3.4 专家推荐意见
数字PCR 可直接定量检测呼吸道标本中病原体个数,适用于低浓度样本、低丰度基因或突变基因的检测,可作其他核酸检测方法的检测限标定。
原博士:数字PCR按照分割单元的方式和结果读取的方式分为微滴数字PCR、芯片数字PCR、微滴芯片数字PCR,技术介绍里少了后2种技术的介绍。
技术特点中强调了主要影响因素是PCR 扩增和荧光信号分析,强调了数字PCR方法和仪器两大主要影响因素,以往大家的关注点都在仪器上,数字PCR方法没有优化好,再好的数字PCR仪也得不到准确的结果。本段落中的“反应单元数越多,灵敏度越高”的表述是错误的,在投入模板量相同的情况下,灵敏度与反应单元数多少无关,当反应单元数远大于模板量时,模板分布服从泊松分布,理论LOD都是3。
性能验证上数字PCR是定量方法,应按照定量检测需验证的性能指标包括:正确度、精密度(包括测量重复性和测量中间精密度)、不确定度、特异度(包括抗干扰能力)、灵敏度、检出限、定量限、线性区间(可报告区间)等。
数字PCR的最低检测限与荧光定量PCR相当,最多低2-3倍,下图中的1 copies/ml的检测限我是不相信的,100-1000 copies/ml是比较合理的。
4 核酸即时检测技术
核酸即时检测为POCT 技术中涉及核酸检测的一大类技术的总称,是核酸提取技术和分子扩增技术(包括实时荧光PCR、巢式PCR、等温扩增、数字PCR等技术)的融和。其最大特点是将核酸的提取、扩增、检测均置于一个反应装置中,通过特定设备对扩增信号检测,完成对靶标核酸的筛查。目前核酸POCT主要以全自动封闭管理系统为主。
4.1 应用场景
主要适用于发热门诊、急诊、ICU 和某些特定病区感染患者的病原体快速检测。与传统POCT 不同,呼吸道病原体核酸POCT 需要对检测病原的生物安全进行评估[14]。流感病毒、肺炎衣原体、肺炎支原体、百日咳杆菌等呼吸道病原体核酸POCT 产品,已作为该类型代表产品问世。
4.2 技术特点
核酸POCT 的灵敏度和特异度高于免疫学POCT,但其成本较高。虽然大部分核酸POCT 产品为封闭体系,但仍需注意PCR 污染的可能性。此外,其检测设备一般较小,便于携带,但也导致其通量较低,不适用于大人群筛查,满足大型医院临床检测需求往往需要配备多组设备。
4.3 性能验证要求
定性检测性能验证指标至少包括:符合率≥90% ;阴性和弱阳性样本精密度检测结果完全一致;靶基因5 次重复检测应100%检出,20 次检测应至少检出18次。
定量检测性能验证指标至少包括:至少 80% 的样本结果偏倚在±7.5%区间内;批内和批间精密度满足说明书范围;线性区间满足说明书范围;20 次检测中≥18 个检测结果与参考值之间的偏倚在±7.5%区间内[8, 11]。
4.4 专家推荐意见
核酸即时检测主要适用于检测场地有限或需要快速筛查的发热门诊、急诊、ICU 等呼吸道感染患者的特定病原体检测。
原博士:POCT是一种技术集成后的表现形式,各种核酸检测技术只要做到集成度高、操作简单、体积小巧样品进结果出都可以叫做POCT,可以是实时荧光PCR、巢式PCR、等温扩增、数字PCR、甚至高通量测序。
PCOT虽然集成度高,但是涉及到核酸扩增环节仍然有污染的风险,因此仍然需要定期加入空白或者环境样品进行污染监测,废弃物密闭独立存放。
性能验证指标写的太简单了,定性应参照实时荧光PCR、定量参照数字PCR。
5 病原体高通量测序技术
病原体高通量测序技术是采用高通量测序技术对临床标本中的核酸进行测序,通过与微生物参考基因组比对获取标本中的微生物物种组成、物种丰度等信息[15]。目前该技术主要分为三类:无偏倚检测的mNGS、检测多重病原体及其耐药基因或毒力基因的tNGS 和获取某一种或多种病原体全基因组数据的高通量测序技术(whole-genome sequencing,WGS)。
5.1 应用场景
由于病原体高通量测序技术复杂、结果解读难度大且价格昂贵,建议根据临床需求在传统微生物检测的基础上选择性使用[16-18],例如,需尽快明确病原学诊断时、目前可及的微生物检验手段无法明确诊断时、出现聚集性呼吸道传染性病例需进行病原体溯源时。
5.2 技术特点
病原体高通量测序技术可对标本中的核酸片段进行物种鉴定,但其物种、耐药基因和毒力基因鉴定的准确性受标本采样、实验操作流程、病原体参考基因组数据库和生物信息学分析等多种因素影响[19]。在临床报告的解读过程中,除深入分析测序数据外,结合患者临床信息及其他实验室数据综合判断和鉴别定植菌与责任病原体亦十分关键[20-21]。
5.3 性能验证要求
实验室在开展病原体高通量测序临床检测前,需参考实验室自建方法的相关要求完成方法学建立和性能确认,结合预期临床用途确立预期性能指标,包括:(1)生信流程评估:最低测序数据量、准确率、召回率、精确率和F1-Score 等;(2)全流程性能确认:背景核酸数据模型、阳性阈值、重复性、最低检测限、抗干扰力、稳定性等;(3)临床评估:对一定数量的真实临床标本进行检测,确定阴性预测价值和阳性预测价值[22-23]。
5.4 专家推荐意见
病原体高通量测序在传统微生物检验未能明确病原或急需快速鉴别是否感染及其病原体时,有选择地使用,主要适用于呼吸道重症感染、疑似特殊病原体感染、聚集性呼吸道传播性感染患者。
原博士:从样本中识别出病原是高通量测序中要求最高的,因为其涉及标本采样、实验操作流程(建库和测序)、病原体参考基因组数据库和生物信息学分析,还涉及到对结果进行专业判读给出致病原,这对专业背景和临床经验的要求很高。目前来看傻瓜式的一键式测序生成结果对于临床检测是不太现实的。
测序的性能验证除了对检测流程还需要对分析数据库和分析流程进行验证,因为生信分析也存在假阳性和假阴性。目前临床上已经出现了一次检测几百种上千种微生物的靶向测序,通过临床样品验证难度极大。

二、成人呼吸道感染病原体核酸检测技术应用建议
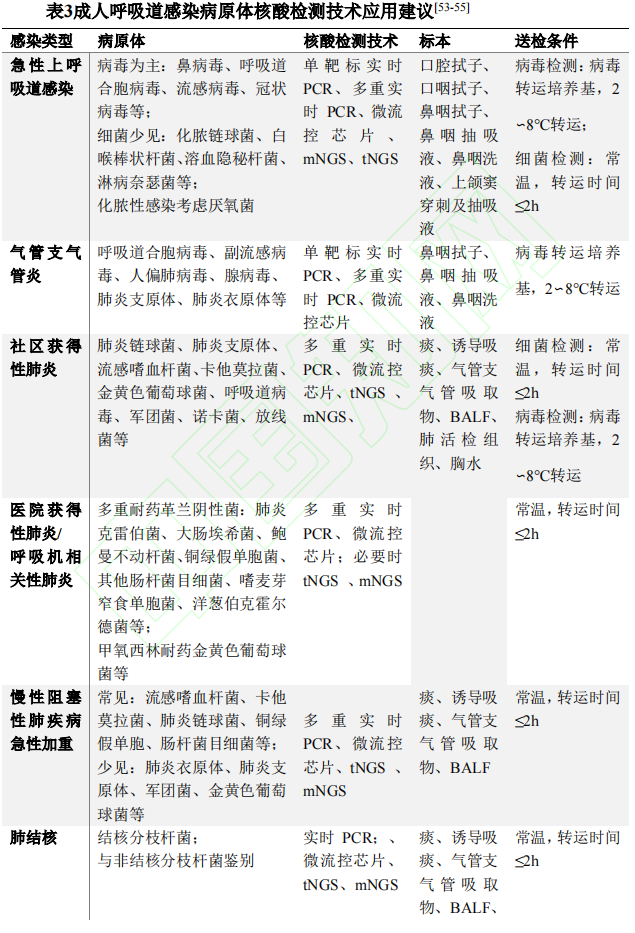

我认为这个专家共识应该是近年来指导性最强的一个文件,文中虽然也出现许多值得商榷的地方,我在文中提出,供大家共同讨论,但是瑕不掩瑜,它对各种技术在不同场景下的使用给出了十分明确建议,对其他行业也有很强的借鉴意义。
来源:中华检验医学培训工程专家委员会、中华医学会呼吸病学分会